Ккоррозия латуни. Коррозионные свойства латуней
В табл. 2 приведены результаты статистической обработки показателей коррозионной агрессивности воды природных источников водоснабжения более чем 30 городов нашей страны.
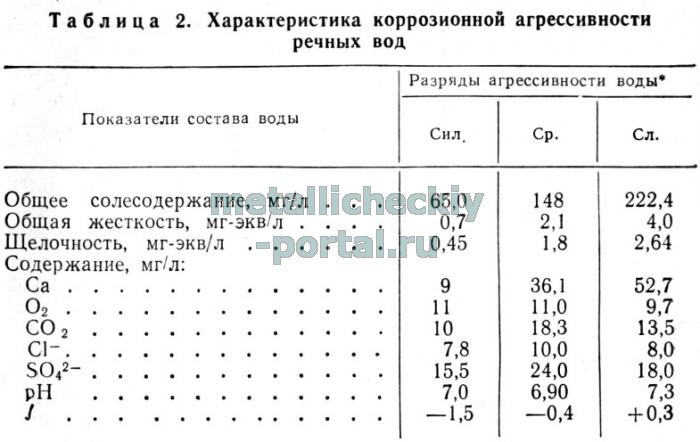
Классификация вод приведена по скорости проникновения коррозии в глубь стальных индикаторов за срок испытания более 1 год. Согласно принятой методике, эта скорость равна 0,002—0,04; 0,04—0,05 и 0,05— 0,2 мм/год; исследованные воды отнесены соответственно к разряду слабо-, средне- и сильноагрессивных.
В деаэрированной почве при нейтральном рН коррозию стальных труб в ней следует ожидать минимальной. Считается, что поглощенный водород затем используется бактериями для уменьшения сульфатов до сульфидов. Согласно этой теории водород удаляется бактериями в процессе, известном как катодная деполяризация, что позволяет продолжать коррозию. В настоящее время считается, что этот механизм, несомненно, играет значительную роль в этом процессе, но он не единственный. Оказывается, что пленка сульфида железа имеет функцию защиты от коррозии, когда она непрерывна.
Роль оксидов и гидроксидов железа и меди при коррозии
В результате скопления оксидов железа в системе может наблюдаться местная коррозия металла. Она имеет вид раковин диаметром, достигающим иногда нескольких десятков миллиметров. Наблюдаемое при протекании этой коррозии утонение металла в пределах раковин — сравнительно равномерное. Раковины в большинстве случаев имеют резко очерченные контуры. Вблизи раковин поверхность трубы часто бывает покрыта рыхлым слоем ржавчин, под которым металл не имеет признаков разрушения. Скорость проникновения коррозии в глубь металла колеблется в значительных пределах: от долей миллиметра до 1 мм в год и более. Основными составляющими наростов, удаленных с поврежденных труб, являются Fe 3 0 4 (до 90%) и СuО (до 10%).
Если это не так, гальваническая коррозия происходит с незакрытым сульфидом металла. Таким образом, бактерии превращают существенно безвредную среду в агрессивную среду, в которой сталь корродирует довольно быстро. Могут быть также другие коррозионные вещества.
Введение новых окислительно-восстановительных реакций В биопленках накопление ионов тяжелых металлов, марганца и железа в концентрациях, значительно превышающих концентрации в объеме среды, может быть на 6 порядков выше. Наличие этих ионов делает новые окислительно-восстановительные реакции доступными для процесса коррозии, особенно катодной реакции.
Испытания прокорродировавших труб показали их пониженную механическую прочность. Травлением дефектных труб в горячем 10%-ном растворе соляной кислоты обнаружена слабая коррозионная стойкость металла, расположенного под слоем шлама. Коррозия под действием оксидов железа труб способна протекать и при наличии, и при отсутствии избыточной щелочности котловой воды.
Генерация клеток кислорода или химических концентраций. В любой биопленке, которая не является смежной, могут генерироваться макроциклы. Оба химических элемента, важные для борьбы с коррозией, также важны для бактериального обмена. Биопленка может быть как источником обоих элементов, так и их хранением. Как правило, биопленка покрывает поверхность металла только в местах, так что могут образовываться кислородные концентраты. В аэрированных средах области металлической поверхности между колиформной структурой биопленки могут контактировать с оксигенированным электролитом.
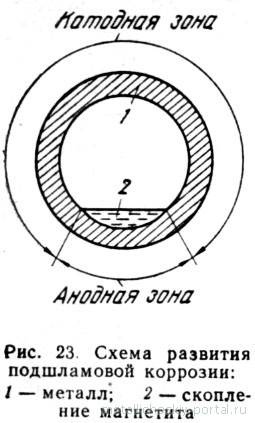
В основе механизма этого вида разрушения металла лежат два процесса: электрохимический и химический. Начальная стадия коррозии развивается с преобладанием электрохимического процесса, обусловленного появлением анодных участков под шламом, образовавшимся на огневой поверхности. Функцию деполяризатора этой коррозионной пары выполняют оксиды трехвалентного железа и меди, расположенные на остальной поверхности труб, играющей роль катода. Скорость проникновения подобной коррозии в глубь металла находится в прямой зависимости от количества поступающих в трубы оксидов железа и меди.
Эти области с относительно высокой концентрацией кислорода внутри биопленки являются катодными для областей с более низкой концентрацией кислорода. Металлическая поверхность под микробной колонией истощается кислородом из-за его метаболического потребления. Кислород нельзя подавать в достаточном количестве из основного объема электролита по двум причинам. Во-первых, диффузия кислорода замедляется барьерным эффектом биопленки, а во-вторых, кислород, проникающий в биопленку, немедленно потребляется в метаболизме.
Образование такой коррозионной ячейки показано на рисунке. Анодный участок расположен под бактериальной колонией, где имеется вмятина. По мере увеличения вмятины железо растворяется в соответствии с анодной реакцией. Нерастворимый гидроксид железа образуется в соответствии с уравнением.
Имеющиеся в трубах повреждения поверхности металла независимо от их природы (коррозионные язвы, глубокие риски и пр.) при поступлении оксидов железа и меди становятся очагами подшламовой коррозии. Различие в химическом составе котловой воды практически не оказывает влияния на развитие коррозии. Отсюда следует, что главной причиной подшламовой коррозии обычно является загрязнение питательной воды оксидами железа и меди.
Коррозионные продукты смешивают с слизистым полимером и образуют клубни, выступающие внутри трубки, которые могут мешать потоку жидкости через трубопровод. Если описанный процесс осуществляется в присутствии бактерий, способных окислять ионы железа до железа, коррозия ускоряется, так как ионы железа удаляются из раствора, как только они образуются. Хлориды, поступающие из основного объема окружающей среды, объединяются с ионами трехвалентного железа, и внутри клубней образуется высококоррозийный раствор хлорида железа.
Другим примером ячейки химической концентрации является ячейка между областями, богатыми марганцем и сульфидами. Когда биопленка возникает одновременно с микробным восстановлением сульфатов и осаждением марганца, вероятно, на поверхности металла образуется дифференциальная потенциальная ячейка. Микробно-опосредованный окислительно-восстановительный цикл марганца сдвигает потенциал открытой поверхности металла до благородных значений, а бактериальное образование сульфида переходит в активное состояние.
Коррозия трубок из медьсодержащих сплавов теплообменных аппаратов
Со стороны охлаждающей воды латунные трубки могут подвергаться общему и местному («пробочному») обесцинкованию, а также ударной коррозии. В некоторых случаях возможна и коррозионная усталость трубок. Обесцинкование латуни — основная форма разрушения конденсаторных трубок, которая представляет собой компонентно-избирательную коррозию цинка, сопровождающуюся вторичным выделением меди в виде рыхлых образований. Вследствие обесцинкования разрушение может носить сплошной характер. При этом металл приобретает хрупкость, трубки легко разрушаются при малейшем механическом воздействии.
Поверхность под сульфидом ведет себя анодно, в то время как площадь под марганцем является катодной. Образование ячейки приводит к локализованной коррозии. Можно ожидать катодный участок, где накапливаются активные микроорганизмы окисления марганца. Для сравнения статьи с дифференциальной аэрацией довольно слабы. Даже с разницей в концентрациях кислорода порядка 10 4 разность потенциалов составляет всего около 60 мВ. Серый чугун характеризуется графитизацией. Серная кислота образуется в результате окисления сульфата в присутствии влаги.
Растворение латуней, как и любых сплавов, образованных компонентами с разными электрохимическими свойствами, начинается с преимущественной ионизации наиболее электроотрицательной составляющей цинка. В случае а-латуней избирательное растворение цинка из объема сплава быстро затухает и затем сплавы растворяются равномерно. р-латуни имеют более высокую концентрацию цинка, поэтому избирательное растворение его создает высокую концентрацию дефектов в поверхностном слое. В определенных условиях за счет поверхностной диффузии на электроде происходит образование мелкодисперсной меди в собственной фа е. Такое избирательное растворение с фазовым превращением на (3-латунях в растворе НС1 протекает частично. Некоторая доля медной составляющей ионизируется и переходит в раствор электролита.
Свежие бытовые сточные воды, поступающие в канализационную систему, содержат значительное количество сульфатов. Как только сульфан проникает через диффузию в свободное пространство над уровнем сточных вод, сернокисляющие аэробные бактерии метаболизируют и окисляют до концентрации до 10% по весу. Это может произойти там, где есть соответствующая подача сульфина, высокая относительная влажность и атмосферный кислород.
Аэробная коррозия В окисленных средах процесс коррозии обычно включает образование кислых метаболитов. Другие микробы генерируют другие типы кислот, например, органические. Коррозионные атаки могут быть как локальными, так и четными. В зависимости от распределения микроорганизмов и метаболитов на поверхности металла. Когда вся бактериальная активность концентрируется на нарушении или расслаивании защитного покрытия, коррозия, вероятно, будет сильно локализована. Однако, если слой метаболитов равномерно распределен по поверхности, коррозия также будет однородной.
Твердый раствор, содержащий больше меди (а-латунь), обычно является катодом по отношению к твердому раствору, содержащему меньше меди (р-латунь). В результате этого в смешанных латунях преимущественно растворяется р-фаза. Часто этот процесс связан с вторичным выделением меди на корродирующей поверхности, т. е. приводит к обесцинкованию. Смешанные а+B-латуни, а также чистые р-латуни более склонны к обесцинкованию, чем латуни с повышенным содержанием меди.
Аэробная коррозия также включает клетки концентрации кислорода. Их функция может способствовать окислению железа в клубнях. В литературе сообщалось о многочисленных других подобных случаях для новых танков и трубопроводов в химической промышленности и атомных электростанциях, где проводились испытания воды с необработанной речной или колодезной водой, и эта вода была оставлена на заводе в течение длительного времени. Аналогичная ситуация может возникнуть со старыми, уже эксплуатируемыми объектами, во время выключения.
Иногда питтинг может сопровождаться трещинами хлоридного коррозионного растрескивания. Общие рекомендации по ограничению проблем коррозии при испытаниях воды для резервуаров и труб из нержавеющей стали заключаются в следующем: для испытания следует использовать конденсат конденсата или конденсата высокой чистоты. После испытания устройство должно быть осушено и высушено как можно скорее. Если необходимо использовать природную воду, ее необходимо фильтровать и хлорировать, а оборудование должно быть высушено или вытерто в течение 3-5 дней после испытания.
В охлаждающей слабоминерализованной воде скорость коррозии изделий из сплава МНЖ 5—1 не превышает 0,01 мм/год. При содержании хлоридов выше 350—400 мг/л коррозия его может достигать 0,05 мм/год. Сплав подвергается язвенной коррозии со скоростью 0,3—0,4 мм/год при вялой циркуляции охлаждающей воды (ниже 0,6 мм/с) и повышенных температурах (более 50°С) на выходе конденсатора. Изделия из сплава МНЖ 5—1 малоустойчивы в высокоминерализованных водах типа морских (срок его эксплуатации не более 8—10 лет). Если в воде присутствуют комплексообразующие ионы — полифосфаты, поверхностно-активные вещества, агрессивное воздействие солевого состава охлаждающей воды на латуни и сплав МНЖ 5—1 усиливается.
Во время полета из-за изменения температуры топливо загрязняется водой. Атака происходит в водной фазе под микробными отложениями и на границе между топливом и водой. Микроорганизмы растут либо в квартирах, либо в клубнях. Микробы, которые обычно считаются основной причиной атаки, производят различные органические кислоты и метаболизируют определенные компоненты топлива. Эти организмы вместе со слизистыми организмами могут образовывать кислородные концентраты под месторождениями. Также можно использовать защитные покрытия, и резервуар часто можно очищать и проводить профилактические осмотры.
Коррозионная агрессивность воды
Водяное охлаждение ферросплавных и электросталеплавильных печей
На предприятиях в наиболее трудных условиях работают системы ферросплавных и электросталеплавильных печей, в теплообменной аппаратуре этих потребителей наблюдается местное кипение воды и интенсивное образование отложений карбоната кальция. Для удаления или предотвращения карбонатных отложений проводят периодическую чистку теплообменной аппаратуры, ее замену, подкисление оборотной воды кислотой, а в последнее время в оборотных системах водоснабжения стали применять химически очищенную воду. Перечисленные средства предотвращения карбонатных отложений имеют существенные недостатки из-за вынужденных простоев металлургических агрегатов в период чистки теплообменной аппаратуры, низкой эффективности метода подкисления оборотной воды и высокой стоимости химически очищенной воды при ее использовании в оборотных системах водоснабжения. Для предотвращения образования отложений предложены новые химические реагенты, относящиеся к классу комплексонов.
Бактериальная слизь применяется при воздействии медных сплавов в пресной речной воде. Совместное действие слизеобразующих бактерий и бактерий, окисляющих железо и марганец, привело к образованию этих отложений. Весьма распространено, что внутренняя поверхность труб и конденсаторов теплообменника из медных сплавов покрыта слоем бактериальной слизи. Если бактерии живы, это только приводит к уменьшению теплопередачи.
Однако, как только они умрут, органические сульфиды начнут разлагаться. Они, как известно, являются коррозионными для медных сплавов. Самый важный шаг в предотвращении - начать с чистой системы и сохранить ее в чистоте. Первое столкновение с устройством биокоррозионного электролита может происходить с гидростатическим тестом на герметичность. Он часто проводится с необработанной речной водой, которая может содержать бактерии, вызывающие коррозию. Поэтому необходимо использовать либо биоциды, либо после тестирования полностью сливать воду и высушить устройство.
Промышленные испытания реагентов на основе комплексонов: оксиэтилидендифосфоновой кислоты (ОЭДФ), нитрилтриметилфосфоновой кислоты (НТФ), ингибитора ДПФ-1, ингибитора ИОМС-1 показали, что по эффективности предотвращения отложений они примерно одинаковы и значительно превосходят традиционные методы стабилизации охлаждающей воды. Эти реагенты способны препятствовать кристаллизации солей из пересыщенных растворов. Их дозировка в обрабатываемой воде не превышает 5 г/м 3 и составляет обычно в зависимости от условий 0,5—3 г/м 3 .
После ввода системы в эксплуатацию успешная профилактика заключается прежде всего в том, чтобы поддерживать чистоту поверхности. Очевидно, что гораздо легче предотвратить распространение микроорганизмов, диспергированных в среде, чем те, которые скрыты в биопленке, нанесенной на поверхность металла. Способы поддержания чистоты систем различны, в зависимости от материала устройства, рабочей среды, экономии энергии и условий рабочего цикла. Наиболее распространенными являются использование покрытий, катодная защита и биоциды.
С самого начала он состоял в основном в обнаружении количества микробов в единице объема воды, взятой из системы. Эти данные были объединены с измерениями электрохимической коррозии, а иногда и с обнаружением потерь на коррозию на образцах доказательств. Поэтому эффективный мониторинг должен включать в себя следующие действия: выявление количества бактерий, нанесенных на поверхность металла, непосредственное наблюдение за идентификацией биопленки структуры бактерий как в химическом анализе воды, так и в биопленке оценки поверхности поверхности морфологии потенциального коррозионного воздействия электрохимической коррозии измерения качества воды и окислительно-восстановительного потенциала.
Медь - тягучий вязкий металл светло-розового цвета, легко прокатывается в тонкие листы, хорошо проводит теплоту и электрический ток. Плотность меди равна 8,96. Общее содержание меди в земной коре составляет 0,01 %. ПДК в воде составляет 0,001 мг/л.
Стандартный электродный потенциал медного электрода для процесса равен +0,52 В, а для процесса составляет +0,337 В. Таким образом, термодинамически более вероятным процессом является образование двухвалентных ионов меди. Обычно при коррозии медь переходит в раствор с образованием. Стационарный потенциал меди в растворе составляет +0,05 В, а в растворе. Поэтому медь в обычных условиях не вытесняет водород из растворов, т.е. не может корродировать с водородной деполяризацией.
Нержавеющие стали - это железо и углеродистые сплавы, содержащие не менее 10, 5% хрома. Нержавеющая сталь часто идентифицируется в виде единого куска, как если бы это был единственный материал. Американский институт железа и стали признает 60 нержавеющих сталей в качестве сплава. Хром является легирующим элементом, который обеспечивает коррозионно-стойкие свойства нержавеющей стали, поскольку в сочетании с кислородом они создают тонкое прозрачное покрытие оксида хрома на поверхности.
Существует 4 основных крупных группы, классифицированных по их металлургической структуре: аустенитная, ферритная, мартенситная и дуплексная. Аустенитные стали используются в рыночных пулах, содержащих от 17 до 25% хрома и от 8 до 10% никеля. Они также содержат несколько элементов для достижения требуемых прочностных свойств. Эти стали обычно не являются магнитными и не притягиваются к магниту.
В растворах комплексообразователей () или окислителей () или даже при продувании через растворы кислорода или воздуха, скорость окисления меди существенно увеличивается (табл.1).
Влияние аэрации кислорода на скорость коррозии меди в кислотах
Окислительные кислоты, такие, как азотная и хромовая, даже разбавленные, вызывают коррозию меди и медных сплавов.
Способность к пассивированию у меди выражена слабо. В атмосферных условиях медь устойчива, на ее поверхности создаются защитные слои типа. Более 50 % меди используется в электротехнической промышленности, 30-40% - для изготовления сплавов, а остальная часть - для изготовления теплообменников, холодильников, вакуумных аппаратов.
Медь со многими металлами дает твердые растворы. Поэтому структура медных сплавов в основном однородна. Медь сообщает сплавам термодинамическую устойчивость. Для медных сплавов характерны те же основные условия протекания коррозионного процесса, что и для чистой меди: они достаточно устойчивы в солевых растворах и в разбавленных неокислительных кислотах. Медь может применяться в промышленности в производстве формалина в колоннах дистилляции, если формалиновые смеси не содержат муравьиной кислоты и в аппараты не попадает воздух. В кипящей смеси формальдегида, воды и метилового спирта скорость коррозии меди не превышает 0,05 мм/год. Медь имеет температуру плавления 1083 °С и не является жаростойким материалом. Однако в некоторых конструкциях она эксплуатируется при повышенных температурах.
Легирование меди другими компонентами может существенно изменить скорость газовой коррозии сплава. Наиболее сильно повышается стойкость меди к газовой коррозии при легировании ее бериллием (до 2,5 %), магнием (до 5 %) и алюминием (до 5%) (рис.1). Для работы при высоких температурах до 900 °С применяют алюминиевые (до) и бериллиевые бронзы.
Латуни - это сплавы меди с цинком (до). Специальные латуни дополнительно легируются и др.
Специальные латуни по коррозионной стойкости не уступают меди. Введение в простую латунь алюминия, марганца или никеля повышает стойкость сплава к атмосферной коррозии, а введение кремния -- в морской воде. Механические свойства, химический состав и области применения латуней и бронз даны в табл.2
Рис. 1 Влияние добавок магния, бериллия и алюминия на скорость окисления меди на воздухе при 800° С.
Латуни широко применяются в качестве материала для труб конденсаторов в паросиловых установках, особенно для корабельных конденсаторов, охлаждаемых быстро протекающей морской водой.
Для простых латуней характерен вид коррозии, который называется обесцинкованием. Латунь на отдельных участках поверхности подвергается специфическому разрушению, в результате которого возникает рыхлый слой меди. Вначале в раствор переходят одновременно цинк и медь. Затем ионы меди вторично выделяются из раствора, а образовавшийся осадок меди, выполняя роль добавочного катода, ускоряет электрохимическую коррозию латуни. В результате в раствор переходят ионы цинка, и с течением времени коррозия распространяется так глубоко, что приводит к образованию сквозных повреждений. Если процесса обесцинкования не происходит, то скорость разрушения латуней в морской воде невелика и составляет.
Для уменьшения обесцинкования латуней сплав дополнительно легируют оловом, никелем, алюминием, а чаще всего мышьяком в количестве.
Латуни в условиях эксплуатации склонны к коррозионному растрескиванию. Это явление наблюдается при наличии в атмосфере аммиака или сернистого ангидрида, а также в растворах, содержащих аммиак, комплексные аммиачные или цианистые соли. Дополнительное легирование латуней небольшими добавками кремния (0,5 %) повышает их стойкость к коррозионному растрескиванию. Кремнистые латуни, содержащие не более при, обладают хорошими механическими и технологическими свойствами.
Для изготовления теплохимических аппаратов чаще всего применяют латуни марок с содержанием марганца и с содержанием олова. Латунь стойка в морской воде, поэтому ее называют "морской латунью" или "адмиралтейским металлом".
Бронзами называют сплавы меди с оловом, а также с алюминием, кремнием, марганцем и т.д.
Оловянистые бронзы содержат не более, чаще - . Они представляют собой твердые растворы. Оловянистые бронзы имеют хорошую коррозионную устойчивость в разбавленных минеральных неокислительных кислотах, в морской воде, в щелочных растворах (исключая аммиачные). Они имеют хорошие антифрикционные свойства и обладают прекрасными литейными качествами.
Алюминиевые бронзы содержат до и имеют однофазную структуру. Эти бронзы стойки в разбавленных растворах кислот, в том числе в соляной, фосфорной, уксусной, лимонной и многих других органических кислотах. Особенно высокой коррозионной стойкостью отличается алюминиевая бронза с содержанием 9,8% А1 и алюминиевая бронза, содержащая дополнительно 4 % железа (Бр.АЖ9-4).
Кремнистые бронзы могут содержать до 15 % кремния, но только при содержании кремния до 3-4 % сплав имеет структуру твердого раствора.
В химической промышленности применяются кремнистые бронзы, дополнительно легированные марганцем (Бр.КМцЗ-1) и никелем (Бр.КН1-3). Они используются для изготовления аппаратуры, работающей под давлением, а также для реакторов взрывоопасных веществ, так как такие бронзы не дают искр при ударе.


 Общероссийский народный фронт: как вступить в организацию?
Общероссийский народный фронт: как вступить в организацию? Сеголен Руаяль: фото, биография, личная жизнь, дети
Сеголен Руаяль: фото, биография, личная жизнь, дети Настоящая француженка кристин лагард Кристин лагард биография семья
Настоящая француженка кристин лагард Кристин лагард биография семья Но не из-за нелепых слов в эфире
Но не из-за нелепых слов в эфире