Характеристика кремния как химического элемента. Химия кремния и его соединения. Сочетание с другими питательными веществами
Кремний (Si) – второй элемент основной (А) подгруппы 4 группы Периодической системы, учрежденной Дмитрием Ивановичем Менделеевым. Кремний очень распространен в природе, поэтому он занимает второе (после кислорода) место по распространенности. Так, без кремния и его соединений не существовало бы Земной коры, которая более чем на четверть состоит из соединений этого химического элемента. В чем же особенности кремния? Каковы формулы его соединений и их применение? Какие важнейшие вещества имеют в своем составе кремний? Попробуем разобраться.
Элемент кремний и его свойства
Кремний существует в природе в нескольких аллотропных модификациях – наиболее распространенными являются кремний в кристаллическом виде и аморфный кремний. Рассмотрим каждую из данных модификаций в отдельности.
Кристаллический кремний
Кремний в данной модификации является темно-серым достаточно твердым и хрупким веществом со стальным блеском. Такой кремний является полупроводником; его полезное свойство заключается в том, что, в отличие от металлов, его электропроводность увеличивается при повышении температуры. Температура плавления такого кремния составляет 1415 °С. К тому же, кристаллический кремний не способен растворяться в воде и различных кислотах.
Применение кремния и его соединений в кристаллической модификации невероятно многообразно. Например, кристаллический кремний входит в состав солнечных батарей, устанавливаемых на космических кораблях и крышах домов. Кремний является полупроводником и способен преобразовывать солнечную энергию в электрическую.
Помимо солнечных батарей, кристаллический кремний используется для создания многих электронных приборов и кремнистых сталей.
Аморфный кремний

Аморфный кремний – бурый/темно-коричневый порошок алмазоподобной структуры. В отличие от кристаллического кремния, данная аллотропная модификация элемента не имеет строго упорядоченной кристаллической решетки. Несмотря на то, что аморфный кремний плавится при температуре, приблизительно равной 1400 °С, он является гораздо более активным по сравнению с кристаллическим. Аморфный кремний не проводит ток и имеет плотность около 2 г/см³.
Такой кремний чаще всего применяется в пищевой промышленности и при изготовлении лекарственных препаратов.
Химические свойства кремния
- Основное химическое свойство кремния – горение в кислороде, в результате которого образуется крайне распространенное соединение – оксид кремния:
Si + O2 → SiO2 (при температуре).
- При нагревании кремний как неметалл образует соединения с различными металлами. Такие соединения называются силицидами. Например:
2Ca + Si → Ca2Si (при температуре).
- Силициды, в свою очередь, без затруднений разлагаются при помощи воды или некоторых кислот. В результате данной реакции образуется особое водородное соединение кремния – газ силан (SiH4):
Mg2Si + 4HCl → 2MgCl2 + SiH4.
- Кремний также способен взаимодействовать с фтором (при нормальных условиях):
Si + 2F2 → SiF4.
- А при нагревании кремний взаимодействует с другими неметаллами:
Si + 2Cl2 → SiCl4 (400–600°).
3Si + 2N2 → Si3N4 (1000°).
Si + C → SiC (2000°).
- Также кремний, взаимодействуя со щелочами и водой, образует соли, называемые силикатами, и газ водород:
Si + 2KOH + H2O → K2SiO3 + H2.
Однако большинство химических свойств данного элемента мы разберем, рассматривая кремний и его соединения, так как именно они являются основными веществами, на которых основано применение и взаимодействие кремния с другими химическими элементами. Итак, какие же соединения кремния являются наиболее распространенными?
Соединения кремния

Ранее мы выяснили, каким элементом является кремний и какими свойствами он обладает. Теперь рассмотрим формулы соединений кремния.
При участии кремния образуется огромное количество различных соединений. Первое место по распространенности занимают кислородные соединения кремния. К данному разряду относится SiO2 и нерастворимая кремниевая кислота.
Кислотный остаток кремниевой кислоты образует различные силикаты (например, CaSiO3 или Al2O3 SiO2). В таких солях и представленных выше соединениях кремния с кислородом элемент имеет типичную для него степень окисления +4.
Также достаточно распространены соли кремния – силициды (Mg2Si, NaSi, CoSi) и соединения кремния с водородом (например, газ силан). Силан, как известно, самовоспламеняется на воздухе с возникновением ослепительной вспышки, а силициды легко разлагаются как при помощи воды, так и различных кислот.
Рассмотрим поподробнее кремний и его соединения, считающиеся самыми распространенными.
Диоксид кремния
Другое название данного оксида – кремнезем. Это твердое и тугоплавкое вещество, которое не растворяется в воде и кислотах и имеет атомную кристаллическую решетку. В природе оксид кремния образует такие минералы и драгоценные камни, как кварц, аметист, опал, агат, халцедон, яшма, кремень и некоторые другие.
Стоит отметить, что именно из кремния первобытные люди изготавливали свои орудия труда и охоты. Кремень положил начало так называемому каменному веку благодаря его повсеместной доступности и способности образовывать острые режущие края при сколе.
Именно оксид кремния делает прочными стебли таких растений, как камыши, тростники и хвощи, листья осоки и стебли злаков. В защитных наружных покровах некоторых животных также содержится кремнезем.
К тому же, он лежит в основе силикатного клея, благодаря которому создается силиконовый герметик и силиконовый каучук.
Химические свойства оксида кремния
Диоксид кремния взаимодействует с огромным количеством химических элементов – как металлов, так и неметаллов. Например:
- При высоких температурах кремнезем взаимодействует со щелочами, образуя при этом соли:
SiO2 + 2KOH → K2SiO3 + H2O (при температуре).
- Как типичный кислотный оксид, данное соединение дает силикаты в результате взаимодействия с оксидами различных металлов:
SiO2 + CaO → CaSiO3 (при температуре).
- Или с карбонатными солями:
SiO2 + K2CO3 → K2SiO3 + CO2 (при температуре).
- Одно из важнейших химических свойств диоксида кремния – это возможность получения из него чистого кремния. Это можно осуществить двумя способами – при взаимодействии диоксида с магнием или углеродом:
SiO2 + 2Mg → 2MgO + Si (при температуре).
SiO2 + 2C → Si + 2CO (при температуре)
Кремниевая кислота

Кремниевая кислота является очень слабой. Она нерастворима в воде и при реакциях образует студенистый осадок, который иногда способен заполнить весь объем раствора. Когда данная смесь высыхает, можно увидеть образовавшийся силикагель, который применяется как адсорбент (поглотитель других веществ).
Наиболее доступный и распространенный способ получения кремниевой кислоты можно выразить при помощи формулы:
K2SiO3 + 2HCl → 2KCl + H2SiO3↓.
Силициды
Рассматривая кремний и его соединения, очень важно сказать о таких его солях, как силициды. Такие соединения кремний образует с металлами, приобретая, как правило, при этом степень окисления -4. Однако такие металлы, как ртуть, цинк, бериллий, золото и серебро не способны взаимодействовать с кремнием и образовывать силициды.
Наиболее распространенными силицидами являются Mg2Si, Ca2Si, NaSi и некоторые другие.
Силикаты
Такие соединения, как силикаты занимают второе место по распространенности после диоксида кремния. Соли-силикаты считаются достаточно сложными веществами, так как имеют непростую структуру строения, а также они входят в состав большинства минералов и горных пород.
К наиболее распространенным в природе силикатам – алюмосиликатам – относят гранит, слюды, различные виды глин. Также известным силикатом является асбест, из которого изготавливаются огнестойкие ткани.
Применение кремния

В первую очередь, кремний применяется для получения материалов-полупроводников и кислотоупорных сплавов. Карбид кремния (SiC) часто используют для затачивания резцов станков и шлифовки ценных камней.
Из расплавленного кварца изготавливается устойчивую и крепкую кварцевую посуду.
Соединения кремния лежат в основе производства стекла и цемента.

Стекла отличаются друг от друга по составу, в котором обязательно присутствует кремний. Например, помимо оконных, существуют тугоплавкие, хрустальные, кварцевые, цветные, фотохромные, оптические, зеркальные и другие стекла.
При смешивании цемента с водой образуется особое вещество – цементный раствор, из которого впоследствии получают такой строительный материал, как бетон.
Производством этих веществ занимается силикатная промышленность. Помимо стекла и цемента, в силикатной промышленности получают кирпич, фарфор, фаянс и различные изделия из них.
Заключение
Итак, мы выяснили, что кремний является важнейшим химическим элементом, широко распространенным в природе. Кремний применяется при строительстве и художественной деятельности, а также незаменим для живых организмов. Многие вещества, начиная от простого стекла и заканчивая ценнейшим фарфором, имеют в своем составе кремний и его соединения.
Изучение химии позволяет познать окружающий наш мир и понять, что не все вокруг, даже самое великолепное и дорогое, настолько таинственно и загадочно, как могло показаться. Желаем успехов в научном познании и изучении такой прекрасной науки, как химия!
Человечество познало кремний достаточно давно. Что такое кремень? Это минерал, который положил, по сути, начало человеческой цивилизации. О лечебных свойствах кремния имеются упоминания в трактатах древних ученых и философов.
Кремний тогда нашел применение для отделки стен в зданиях, где хранилось мясо и мясопродукты, для вырезания бородавок, для присыпки ран в виде порошка, что позволяло предотвратить гангрену; кремниевыми жерновами производили муку с превосходными вкусовыми и хлебопекарными качествами.
Издревле люди выкладывали внутреннюю поверхность и дно колодцев кремнием, поскольку было замечено, что употребление воды из таких колодцев обеспечивало профилактику соматических и инфекционных заболеваний, а вода оказалась необыкновенно вкусная, прозрачная и целебная. Дело в том, что кремень при соприкосновении с водой изменяет ее свойства.
Лечебные свойства кремния и причины дефицита в организме
Клинические наблюдения современных ученых доказали, что кремний в воде вырабатывает кремниевую кислоту. Дозы этого соединения  весьма малы, но вполне достаточные для того, чтобы кремниевая кислота растворяла отложения солей и шлаки, а также выводила их из организма.
весьма малы, но вполне достаточные для того, чтобы кремниевая кислота растворяла отложения солей и шлаки, а также выводила их из организма.
Вода под влиянием кремния становится «живой» и обновленной. Биологически активные вещества кремния в нашем организме вместе с белковыми фракциями способствуют образованию гормонов, аминокислот, ферментов; обратите внимание на то, что около 70 видов витаминов и минералов не усваивается, когда в организме не хватает кремния.
_________________________________________________________________________
Причины дефицита кремния
» Недостаточное употребление минеральной воды и клетчатки.
» Избыточное количество алюминия (это обычно бывает у людей, готовивших пищу в алюминиевой посуде).
» Интенсивный рост организма в детском возрасте.
» Повышенные физические и умственные нагрузки каждый день.
Что происходит при нехватке кремния
» Прогрессируют течение .
» В почках, печени и желчном пузыре складывается тенденция к .
» У пациента начинаются , и зубов, ломкость ногтей.
» Возникают болезни глаз: у пожилых людей – дальнозоркость, глаукома и катаракта, у детей – .
» Поражаются все кровеносные сосуды с развитием раннего , повышением .
» Из-за нарушения состояния соединительной ткани возникают пародонтоз, деформирующий и .
Кремний – источник крепкого здоровья
Теперь уже известно, что кремниевая вода повышает защитные силы органума, нормализует обмен веществ, предупреждает возникновение многих заболеваний и способствует их излечению, замедляет старение организма.
При наружном применении кремниевой воды омолаживается кожа, улучшается состояние и рост волос, исчезают морщины, улучшается цвет рук и лица.
Как пить кремниевую воду. Ее можно употреблять без ограничений. Обычно кремниевую воду пьют от одного до трех стаканов комнатной температуры, но пить нужно небольшими глотками. Как отмечено выше, кремний изменяет свойства воды при соприкосновении с ней.
Активированная кремниевая воды оказывает губительное действие на патогенные микроорганизма, снижает рост бактерий, которые способствуют брожению и гниению. При этом вода становится приятной на вкус и идеально чистой, долгое время она не портится, приобретая многие другие лечебные свойства. Кремний вытесняет соли тяжелых и вредных металлов, они осаждаются на дно, а сверху остается чистая вода.
Всем известно насколько нужна вода человеческому организму. В нем около 70% воды и невозможно представить жизнь без нее. Учитывая, что все процессы обмена веществ происходят в присутствии водной среды, можно с уверенностью сказать, что именно вода играет роль проводника большого количества физиологических процессов, без нее невозможна жизнедеятельность клетки и тканей.
Как приготовить кремниевую воду
 Настаивать кремний рекомендуется в эмалированной или стеклянной посуде. Лично я готовлю кремниевую воду в домашних условиях в трёхлитровой стеклянной банке. Кладу в баночку камешки кремния, наливаю чистую колодезную воду (если вы живете в городе, лучше перед этим ее профильтровать через обычный домашний фильтр).
Настаивать кремний рекомендуется в эмалированной или стеклянной посуде. Лично я готовлю кремниевую воду в домашних условиях в трёхлитровой стеклянной банке. Кладу в баночку камешки кремния, наливаю чистую колодезную воду (если вы живете в городе, лучше перед этим ее профильтровать через обычный домашний фильтр).
Банку ставлю в комнате, где не опадают прямые солнечные лучи и покрываю обычной марлевой салфеткой (куском марли) для обеспечения свободного газообмена. Кремниевую воду, применяемую для приготовления чая, пищи или настоев лекарственных растений, настаиваю два-три дня. При этом следует соблюдать следующие требования:
- После каждого сливания воды кремний и емкость тщательно промывать проточной водой.
- Оставшийся на дне осадок нужно вылить в раковину.
- Настоянную на кремне воду кипятить разрешается, но не сам кремень, потому что вода в таком случае перенасыщается биологически активными веществами. Такую воду применять можно только наружно.
- Вместе с кремнием воду хранить в холодильнике не рекомендуется.
- Установлено, что кремниевая вода сохраняет целебные свойства в течение нескольких месяцев.
- После неоднократного использования (3-5 раз) кремний следует промыть под проточной водой и выставить на свежем воздухе на 2 часа для проветривания.
- Через какое-то определенное время на поверхности минералов могут появиться налеты или наслоения. В таком случае камешки надо поместить на два часа в подсоленную воду или 2% раствор уксусной кислоты, после чего промыть проточной водой. Далее опустить камни опять на два часа в раствор пищевой соды и снова промыть под краном.
- Месяцев через 8-12 желательно камешки расколоть, чтобы усилить (обновить) их свойства, но лучше приобрести новые минерал.
- Настаивание кремния проводится при комнатной температуре.
Будьте здоровы, дорогие мои читатели. Дай вам Бог!
Многие современные технологические устройства и аппараты были созданы за счет уникальных свойств веществ, находящихся в природе. Человечество экспериментальным путем и тщательным изучением окружающих нас элементов постоянно модернизирует собственные изобретения - данный процесс называется техническим прогрессом. Он основан на элементарных, доступных каждому вещах, которые окружают нас в повседневной жизни. Например, песок: что может быть в нем удивительного и необычного? Ученые смогли выделить из него кремний - химический элемент, без которого не существовало бы компьютерной техники. Область его применения отличается разнообразием и постоянно расширяется. Это достигается за счет уникального свойства атома кремния, его структуры и возможности соединений с другими простыми веществами.
Характеристика
В разработанной Д. И. Менделеевым, кремний обозначен символом Si. Относится к неметаллам, располагается в главной четвертой группе третьего периода, имеет атомный номер 14. Его соседство с углеродом не является случайным: во многом их свойства сопоставимы. В природе не встречается в чистом виде, так как является активным элементом и имеет достаточно прочные связи с кислородом. Основное вещество - кремнезем, который является оксидом, и силикаты (песок). При этом кремний (его природные соединения) является одним из наиболее распространенных химических элементов на Земле. По массовой доле содержания он занимает второе место после кислорода (более 28 %). Верхний слой земной коры содержит кремний в виде диоксида (это кварц), различные типы глин и песка. Вторую по распространенности группу составляют его силикаты. На глубине около 35 км от поверхности расположены слои гранита и базальтовые отложения, в состав которых входят кремневые соединения. Процент содержания в земном ядре пока не просчитан, но ближайшие к поверхности слои мантии (до 900 км) содержат силикаты. В составе морской воды концентрация кремния составляет 3 мг/л, на 40 % состоит из его соединений. Просторы космоса, которые человечество на сегодняшний день изучило, содержат этот химический элемент в больших количествах. Например, метеоритов, которые приближались к Земле на расстояние, доступное исследователям, показал, что они состоят на 20 % из кремния. Существует вероятность формирования жизни на основе этого элемента в нашей галактике.

Исследовательский процесс
История открытия химического элемента кремния имеет несколько этапов. Многие вещества, систематизированные Менделеевым, использовались человечеством на протяжении веков. При этом элементы находились в природном виде, т.е. в соединениях, которые не подвергались химической обработке, и все их свойства не были известны людям. В процессе изучения всех особенностей вещества у него появлялись новые направления использования. Свойства кремния на сегодняшний день не изучены до конца - этот элемент при достаточно широком и разнообразном спектре применения оставляет простор для новых открытий будущим поколениям ученых. Современные технологии значительно ускорят данный процесс. В XIX веке многие знаменитые химики пытались получить кремний в чистом виде. Впервые это удалось сделать Л. Тенару и Ж. Гей-Люссаку в 1811 году, но открытие элемента принадлежит Й. Берцелиусу, который смог не только выделить вещество, но и описать его. Химик из Швеции получил кремний в 1823 году, для этого он использовал металлический калий и калиевую соль. Реакция происходила при катализаторе в виде высокой температуры. Полученное простое вещество серо-бурого цвета являло собой аморфный кремний. Кристаллический чистый элемент был получен в 1855 году Сент-Клер Девилем. Сложность выделения напрямую связана с высокой прочностью атомных связей. В обоих случаях химическая реакция направлена на процесс очищения от примесей, при этом аморфная и кристаллическая модели имеют разные свойства.

Кремний: произношение химического элемента
Первое название полученного порошка - кизель - было предложено Берцелиусом. В Великобритании и США кремний и по сей день называют не иначе, как силиций (Silicium) или силикон (Silicon). Термин происходит от латинского «кремень» (или «камень»), и в большинстве случаев его привязывают к понятию «земля» за счет широкого распространения в природе. Русское произношение данного химического вещества бывает разное, все зависит от источника. Его называли кремнеземом (Захаров применял такой термин в 1810 г.), сицилием (1824 год, Двигубский, Соловьев), кремнеземнием (1825 год, Страхов), и только в 1834 году российский химик Герман Иванович Гесс вводит наименование, которое до сегодняшнего момента используется в большинстве источников - кремний. В он обозначен символом Si. Как читается химический элемент кремний? Многие ученые англоязычных стран произносят его наименование как «си» или употребляют слово «силикон». Отсюда происходит известное на весь мир название долины, которая является научно-исследовательской и производственной площадкой компьютерной техники. Русскоязычное население называет элемент кремнием (от древнегреческого слова «утес, гора»).
Нахождение в природе: месторождения
Целые горные системы сложены из соединений кремния, который в чистом виде не встречается, ведь все известные минералы являются диоксидами или силикатами (алюмосиликатами). Удивительные по красоте камни используются людьми в качестве поделочного материала - это опалы, аметисты, кварцы различных типов, яшма, халцедон, агат, горный хрусталь, сердолик и многие другие. Образовались они благодаря вхождению в состав кремния различных веществ, которые определили их плотность, структуру, цвет и направление использования. Весь неорганический мир можно связать с этим химическим элементом, который в природной среде образует прочные связи с металлами и не металлами (цинк, магний, кальций, марганец, титан и т. д.). По сравнению с другими веществами, кремний достаточно легкодоступен для добычи в производственных масштабах: он содержится в большинстве видов руды и минералов. Поэтому активно разрабатываемые месторождения привязываются скорее к доступным источникам энергии, чем к территориальным скоплениям вещества. Кварциты и кварцевые пески есть во всех странах мира. Наиболее крупными производителями и поставщиками кремния являются: Китай, Норвегия, Франция, США (Западная Вирджиния, Огайо, Алабама, Нью-Йорк), Австралия, ЮАР, Канада, Бразилия. Все изготовители используют различные способы, которые зависят от вида выпускаемой продукции (технический, полупроводниковый, высокочастотный кремний). Химический элемент, дополнительно обогащенный или, наоборот, очищенный от всех видов примесей, имеет индивидуальные свойства, от которых зависит его дальнейшее использование. Это относится и к данному веществу. Строение кремния определяет сферу его применения.

История использования
Очень часто из-за схожести наименований люди путают кремний и кремень, однако понятия эти не тождественны. Внесем ясность. Как уже упоминалось, в природе кремний в чистом виде не встречается, чего нельзя сказать о его соединениях (тот же кремнезем). Основные минералы и горные породы, образуемые диоксидом рассматриваемого нами вещества — это песок (речной и кварцевый), кварц и кварциты, и кремень. О последнем слышали, должно быть, все, ведь ему придается большое значение в истории развития человечества. С данным камнем связывают первые орудия труда, созданные людьми в период каменного века. Его острые грани, образующиеся при откалывании от основной породы, значительно облегчали труд древних домохозяек, а возможность заострения - охотников и рыболовов. Кремень не обладал прочностью металлических изделий, но вышедшие из строя инструменты было легко заменить новыми. Его использование в качестве огнива продолжалось многие века - вплоть до изобретения альтернативных источников.
Что касается современных реалий, свойства кремния позволяют эксплуатировать вещество для отделки помещений или создания керамической посуды, при этом, помимо прекрасного эстетичного вида, он имеет множество отличных функциональных качеств. Отдельное направление его применения связано с изобретением стекла около 3000 лет назад. Это событие дало возможность создавать зеркала, посуду, мозаичные витражи из соединений, содержащих кремний. Формула начального вещества дополнялась необходимыми составляющими, что позволяло придавать изделию требуемый цвет и влияло на прочность стекла. Удивительные по красоте и разнообразию произведения искусства были сделаны человеком из минералов и камней, содержащих кремний. Целебные свойства этого элемента были описаны учеными древности и применялись на протяжении всей истории человечества. Им выкладывали колодцы для питьевой воды, кладовые для хранения продуктов, использовали как в быту, так и в медицине. Порошок, полученный в результате измельчения, прикладывали к ранам. Особое внимание уделялось воде, которая настаивалась в посуде, сделанной из соединений, содержащих кремний. Химический элемент взаимодействовал с ее составом, что позволяло уничтожать ряд болезнетворных бактерий и микроорганизмов. И это еще далеко не все отрасли, где рассматриваемое нами вещество весьма и весьма востребовано. Строение кремния обуславливает его многофункциональность.

Свойства
Для более подробного ознакомления с особенностями вещества его необходимо рассмотреть с учетом всех возможных свойств. План характеристики химического элемента кремния включает в себя физические свойства, электрофизические показатели, изучение соединений, реакции и условия их прохождения и т. д. Кремний в кристаллической форме имеет темно-серый с металлическим отливом цвет. Решетка гранецентрированная кубическая имеет сходство с углеродной (алмаз), но за счет большей длины связей не настолько прочная. Пластичным её делает нагревание до 800 о С, в остальных случаях она остается хрупкой. Физические свойства кремния делают это вещество поистине уникальным: он является прозрачным для инфракрасного излучения. Температура плавления - 1410 0 С, кипения - 2600 0 С, плотность при нормальных условиях - 2330 кг/м 3 . Теплопроводность непостоянна, для различных образцов она принимается в приблизительном значении 25 0 С. Свойства атома кремния позволяют использовать его в качестве полупроводника. Это направление применения наиболее востребовано в современном мире. На величину электропроводности оказывает влияние состав кремния и элементы, находящиеся в соединении с ним. Так, для повышенной электронной проводимости используются сурьма, мышьяк, фосфор, для дырчатой - алюминий, галлий, бор, индий. При создании приборов с кремнием в качестве проводника применяется поверхностная обработка определенным агентом, который и оказывает влияние на работу аппарата.
Свойства кремния как отличного проводника используются достаточно широко в современном приборостроении. Особенно актуально его применение при производстве сложной техники (например, современные вычислительные устройства, компьютеры).
Кремний: характеристика химического элемента
В большинстве случаев кремний четырехвалентен, также встречаются связи, в которых он может иметь значение +2. При нормальных условиях он малоактивен, имеет прочные соединения, при комнатной температуре может вступить в реакцию только со фтором, находящимся в газообразном агрегатном состоянии. Это объясняется эффектом блокирования поверхности диоксидной пленкой, который наблюдается при взаимодействии с окружающим кислородом или водой. Для стимуляции реакций необходимо применять катализатор: повышение температуры идеально подходит для такого вещества, как кремний. Химический элемент взаимодействует с кислородом при 400-500 0 С, в результате диоксидная пленка увеличивается, идет процесс окисления. При повышении температуры до 50 0 С наблюдается реакция с бромом, хлором, йодом, в результате чего образуются летучие тетрагалогениды. С кислотами кремний не взаимодействует, исключение составляет смесь фтористоводородной и азотной, при этом любая щелочь в нагретом состоянии является растворителем. Кремневодороды образуются только путем разложения силицидов, в реакцию с водородом он не вступает. Наибольшей прочностью и химической пассивностью отличаются соединения с бором и углеродом. Высокую стойкость по отношению к щелочам и кислотам имеет соединение с азотом, которое происходит при температуре свыше 1000 0 С. Силициды получаются при реакции с металлами, и в этом случае от дополнительного элемента зависит валентность, которую показывает кремний. Формула вещества, образованного при участии переходного металла, является стойкой к воздействию кислот. Строение атома кремния напрямую влияет на его свойства и способность взаимодействовать с другими элементами. Процесс образования связей в природе и при воздействиях на вещество (в лабораторных, промышленных условиях) различается значительно. Строение кремния предполагает его химическую активность.
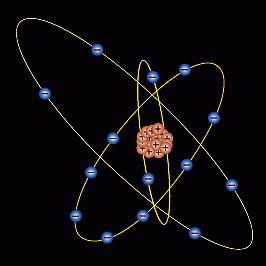
Строение
Кремния имеет свои особенности. Заряд ядра +14, что соответствует порядковому номеру в периодической системе. Количество заряженных частиц: протонов - 14; электронов - 14; нейтронов - 14. Схема строения атома кремния имеет следующий вид: Si +14) 2) 8) 4. На последнем (внешнем) уровне расположено 4 электрона, что определяет степень окисления со знаком «+» или «-». Оксид кремния имеет формулу SiO 2 (валентность 4+), летучее водородное соединение - SiH 4 (валентность -4). Большой объем атома кремния позволяет в некоторых соединениях иметь координационное число 6, например, при соединении со фтором. Молярная масса - 28, радиус атома - 132 пм, конфигурация электронной оболочки: 1S 2 2S 2 2P 6 3S 2 3P 2 .
Применение
Поверхностно или полностью легированный кремний используется в качестве полупроводника при создании многих, в том числе высокоточных, приборов (например, солнечные фотоэлементы, транзисторы, выпрямители тока и т. д.). Сверхчистый кремний применяется для создания солнечных батарей (энергетика). Монокристаллический вид используется для изготовления зеркал и газового лазера. Из соединений кремния получают стекло, керамическую плитку, посуду, фарфор, фаянс. Многообразие получаемых видов товаров описать сложно, их эксплуатация происходит на бытовом уровне, в искусстве и науке, на производстве. Получаемый цемент служит сырьем для создания строительных смесей и кирпича, отделочных материалов. Распространение масел, смазки на основе позволяет значительно уменьшить силу трения в подвижных частях многих механизмов. Силициды за счет уникальных свойств в области противодействия агрессивным средам (кислотам, температурам) широко применяются в промышленности. Их электрические, ядерные и химические показатели принимают во внимание специалисты на сложных производствах, не последнюю роль играет и строение атома кремния.
Мы перечислили самые наукоемкие и передовые на сегодняшний день сферы применения. Наиболее распространенный, изготавливаемый в больших объемах технический кремний используется по целому ряду направлений:
- В качестве сырья для производства более чистого вещества.
- Для легирования сплавов в металлургической промышленности: наличие кремния увеличивает тугоплавкость, повышает устойчивость к коррозии и механическую прочность (при избытке данного элемента сплав может оказаться слишком хрупким).
- В качестве раскислителя для удаления лишнего кислорода из металла.
- Сырье для производства силанов (соединений кремния с органическими веществами).
- Для производства водорода из сплава кремния с железом.
- Изготовление солнечных батарей.

Велико значение данного вещества и для нормального функционирования организма человека. Строение кремния, его свойства являются в данном случае определяющими. При этом переизбыток или недостаток его ведет к серьезным заболеваниям.
В организме человека
Медицина достаточно давно использует кремний в качестве бактерицидного и антисептического средства. Но при всей пользе наружного применения данный элемент должен постоянно возобновляться в организме человека. Нормальный уровень его содержания позволит улучшить жизнедеятельность в целом. В случае его недостатка более 70 микроэлементов и витаминов не будут усвоены организмом, что значительно понизит сопротивляемость к целому ряду заболеваний. Наибольшее процентное соотношение кремния наблюдается в костях, коже, сухожилиях. Он играет роль структурного элемента, который поддерживает прочность и придает упругость. Все скелетные твердые ткани формируются за счет его соединений. В результате последних исследований обнаружено содержание кремния в почках, поджелудочной железе и соединительных тканях. Роль данных органов в функционировании организма достаточно велика, поэтому снижение его содержания губительно отразится на многих основных показателях жизнеобеспечения. В сутки с пищей и водой организм должен получать 1 грамм кремния - это поможет избежать возможных болезней, таких как воспалительные процессы кожного покрова, размягчение костей, образование камней в печени, почках, ухудшение зрения, состояния волос и ногтей, атеросклероз. При достаточном уровне содержания данного элемента повышается иммунитет, нормализуются обменные процессы, улучшается усвоение многих элементов, необходимых для здоровья человека. Наибольшее количество кремния - в злаковых культурах, редисе, гречневой крупе. Значительную пользу принесет кремниевая вода. Для определения количества и частоты ее использования лучше проконсультироваться со специалистом.
Химический элемент
Кремний - химический элемент № \(14\). Он расположен в IVА группе Периодической системы.
Si 14 + 14) 2e) 8e) 4e
На внешнем слое атома кремния содержатся четыре валентных электрона. До его завершения не хватает четырёх электронов. Поэтому в соединениях с металлами кремнию характерна степень окисления \(–4\), а при взаимодействии с более электроотрицательными неметаллами он проявляет положительные степени окисления \(+2\) или \(+4\).
По содержанию в земной коре кремний занимает второе место после кислорода. Земная кора более чем наполовину образована соединениями кремния. Распространены оксид кремния (IV ) Si O 2 , силикаты и алюмосиликаты . Песок, кварц, горный хрусталь, аметист состоят из оксида. Гранит, полевой шпат, глина представляют собой силикаты и алюмосиликаты.
Входит кремний и в состав живых организмов. Его соединения придают прочность стеблям растений, содержатся в наружных покровах животных, образуют раковины и скелеты некоторых обитателей водной среды. У человека кремний присутствует в волосах и ногтях.
Скелеты радиолярий
Простое вещество
Кремний имеет атомную кристаллическую решётку, похожую на решётку алмаза. Каждый атом кремния в его кристаллах связан четырьмя ковалентными связями с соседними атомами. Благодаря такому строению у него высокая твёрдость.
Радиус атома кремния больше радиуса атома углерода, поэтому в его кристаллах электроны более свободны по сравнению с алмазом. Кремний проводит электрический ток, а его электропроводность увеличивается с повышением температуры или при освещении. Такие вещества относятся к полупроводникам .
В отличие от алмаза кремний представляет собой чёрно-серое непрозрачное вещество. У него высокая температура плавления (\(1428\) °С).
Кремний
Получают кремний восстановлением его оксида коксом в электропечах:
Si O 2 + 2C = t Si + 2CO .
Химические свойства
В химических реакциях кремний может проявлять и окислительные , и восстановительные свойства. Окислительные свойства кремния выражены слабее, чем у остальных неметаллов.
- Взаимодействие с металлами.
При высокой температуре кремний реагирует с металлами с образованием силицидов :
2Mg 0 + Si 0 = t Mg + 2 2 Si − 4 .
В этой реакции кремний - окислитель .
- С водородом не реагирует.
С водородом кремний практически не реагирует по причине неустойчивости водородного соединения силана Si H 4 . Силан можно получить при гидролизе силицидов:
Mg 2 Si + 4H 2 O = 2Mg (OH) 2 ↓ + Si H 4 .
Он самовоспламеняется на воздухе и сгорает с образованием оксида кремния(\(IV\)) и воды:
Si H 4 + 2O 2 = Si O 2 + 2H 2 O .
- Взаимодействие с кислородом.
Кремний горит в кислороде и проявляет в этой реакции восстановительные свойства.
Кремний (Si) - это неметалл, стоящий на 2 месте после кислорода по запасам и нахождению на Земле(25,8% в Земной коре). В чистом виде он практически не встречается, в основном присутствует на планете в виде соединений.
Характеристика кремния
Физические свойства

Кремний - это хрупкий светло-серый материал с металлическим оттенком или порошкообразный материал коричневого цвета. Строение кристалла кремния однотипно с алмазом, но из-за различий в длине связи между атомами твердость алмаза значительно выше.
Кремний - неметалл, доступный для электромагнитного излучения. Благодаря некоторым качествам, он находится в середине между неметаллами и металлами:
При увеличении температуры до 800 °C становится гибким и пластичным;
При нагревании до 1417 °С плавится;
Начинает кипеть при температуре свыше 2600 °С;
Меняет плотность при высоком давлении;
Обладает свойством намагничиваться против направления внешнего магнитного поля (диамагнит).
Кремний - полупроводник, и примеси, входящие в его сплавы определяют электрические характеристики будущих соединений.
Химические свойства

При разогревании Si вступает в реакцию с кислородом, бромом, йодом, азотом, хлором и различными металлами. При соединении с углеродом получаются твердые сплавы с термо - и химио - стойкостью.
Кремний никак не воздействует с водородом, поэтому все возможные смеси c ним получают другим путем.
При обычных условиях он слабо реагирует со всеми веществами, кроме газообразного фтора. С ним образуется тетрафторид кремния SiF4. Такая неактивность объясняется тем, что на поверхности неметалла из-за реакции с кислородом, водой, ее парами и воздухом ложится пленка диоксида кремния и окутывает его. Поэтому химическое воздействие замедленно и незначительно.
Для удаления этого слоя используют смесь фтороводородной и азотной кислот или водные растворы щелочей. Некоторые специальные жидкости для этого предусматривают добавление хромового ангидрида и иных веществ.
Нахождение кремния в природе

Кремний для Земли столь же важен как углерод для растений и животных. Ее кора почти наполовину состоит из кислорода, а если добавить к этому кремний, получится 80% массы. Эта связь очень важна для перемещения химических элементов.
75% литосферы содержат различные соли кремневых кислот и минералов (песок, кварциты, кремень, слюды, полевые шпаты и т. д.). Во время образования магмы и разных магматических пород Si накапливается в гранитах и в ультраосновных породах (плутонических и вулканических).
В теле человека 1 г кремния. Большинство содержится в костях, сухожилиях, кожном и волосяном покрове, лимфоузлах, аорте и трахее. Он участвует в процессе роста соединительной и костной тканей, а так же поддерживает эластичность сосудов.
Норма употребления в день для взрослого - 5 - 20 мг. Избыток вызывает силикоз.
Применение кремния в промышленности

С каменного века этот неметалл известен человеку и широко используется до сих пор.
Применение:
Он хороший восстановитель, поэтому его используют в металлургии для получения металлов.
В определенных условиях кремний способен проводить электричество, поэтому его применяют в электронике.
Оксид кремния используется в изготовлении стекол и силикатных материалов.
Специальные сплавы используется для производства полупроводниковых приборов.


 Общероссийский народный фронт: как вступить в организацию?
Общероссийский народный фронт: как вступить в организацию? Сеголен Руаяль: фото, биография, личная жизнь, дети
Сеголен Руаяль: фото, биография, личная жизнь, дети Настоящая француженка кристин лагард Кристин лагард биография семья
Настоящая француженка кристин лагард Кристин лагард биография семья Но не из-за нелепых слов в эфире
Но не из-за нелепых слов в эфире